|
细胞骨架(cytoskeleton)是指真核细胞中的蛋白纤维网络结构。发现较晚,主要是因为一般电镜制样采用低温(0-4℃)固定,而细胞骨架会在低温下解聚。直到20世纪60年代后,采用戊二醛常温固定,才逐渐认识到细胞骨架的客观存在。
细胞骨架不仅在维持细胞形态,承受外力、保持细胞内部结构的有序性方面起重要作用,而且还参与许多重要的生命活动(图9-1),如:在细胞分裂中细胞骨架牵引染色体分离,在细胞物质运输中,各类小泡和细胞器可沿着细胞骨架定向转运;在肌肉细胞中,细胞骨架和它的结合蛋白组成动力系统;在白细胞的迁移、精子的游动、神经细胞轴突和树突的伸展等方面都与细胞骨架有关。另外,在植物细胞中细胞骨架指导细胞壁的合成。
细胞骨架由微丝(microfilament)、微管(microtubule)和中间纤维(intemediate filament)构成。微丝确定细胞表面特征,使细胞能够运动和收缩。微管确定膜性细胞器(membrane-enclosed organelle)的位置和作为膜泡运输的导轨。中间纤维使细胞具有张力和抗剪切力。
微丝、微管和中间纤维位于细胞质中,又称胞质骨架,它们均由单体蛋白以较弱的非共价键结合在一起,构成纤维型多聚体,很容易进行组装和去组装,这正是实现其功能所必需的特点。
广义的细胞骨架还包括核骨架(nucleoskeleton)、核纤层(nuclear lamina)和细胞外基质(extracellular matrix),形成贯穿于细胞核、细胞质、细胞外的一体化网络结构。
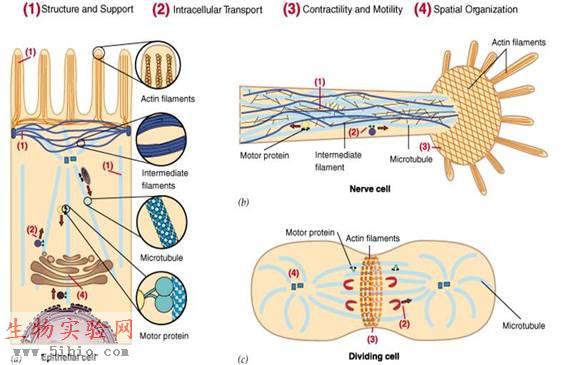
图9-1 细胞骨架的主要功能(图片来自 G. Karp 2002)
第一节 微丝
微丝(microfilament,MF)是由肌动蛋白(actin)组成的直径约7nm的骨架纤维,又称肌动蛋白纤维actin filament。微丝和它的结合蛋白(association protion)以及肌球蛋白(myosin)三者构成化学机械系统,利用化学能产生机械运动。
一、分子结构
根据等电点的不同可将高等动物细胞内的肌动蛋白分为3类,α分布于各种肌肉细胞中,β和γ分布于肌细胞和非肌细胞中。
肌动蛋白纤维是由两条线性排列的肌动蛋白链形成的螺旋,状如双线捻成的绳子(图9-2、3),肌动蛋白的单体为球形分子,称为球形肌动蛋白G-actin(globular actin),它的多聚体称为纤维形肌动蛋白F-actin (fibrous actin)。
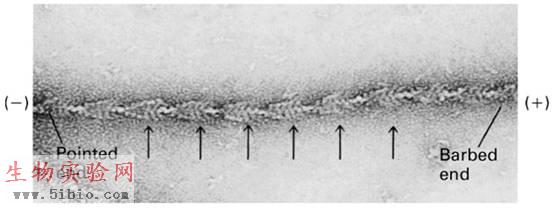
图9-2 微丝纤维的负染电镜照片

图9-3 微丝纤维结构模型
肌动蛋白在进化上高度保守,酵母和兔子肌肉的肌动蛋白有88%的同源性。不同类型肌肉细胞的α-肌动蛋白分子一级结构(约400个氨基酸残基)仅相差4~6个氨基酸残基,β-肌动蛋白或γ-肌动蛋白与α-横纹肌肌动蛋白相差约25个氨基酸残基。
多数简单的真核生物,如酵母或粘菌,含单个肌动蛋白基因,仅合成一种肌动蛋白。真核生物含有多个肌动蛋白基因,如海胆有11个,网柄菌属(Dictyostelium)有17个,在某些植物中有60个。肌动蛋白要经过翻译后修饰,如N-端乙酰化或组氨酸残基的甲基化。
在适宜的温度,存在ATP、K+、Mg2+离子的条件下,肌动蛋白单体可自组装为纤维。
ATP-actin(结合ATP的肌动蛋白)对微丝纤维末端的亲和力高,ADP-actin对纤维末端的亲和力低,容易脱落。当溶液中ATP-actin浓度高时,微丝快速生长,在微丝纤维的两端形成ATP-actin“帽子”,这样的微丝有较高的稳定性。伴随着ATP水解,微丝结合的ATP就变成了ADP,当ADP-actin暴露出来后,微丝就开始去组装而变短。
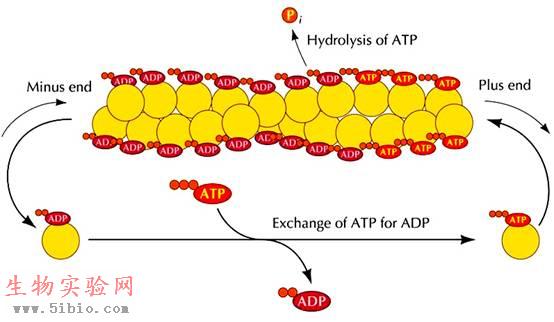
图9-4 肌动蛋白的踏车行为
微丝具有极性,肌动蛋白单体加到(+)极的速度要比加到(-)极的速度快5-10倍。溶液中ATP-肌动蛋白的浓度也影响组装的速度。当处于临界浓度时,ATP-actin可能继续在(+)端添加、而在(-)端开始分离,表现出一种“踏车”现象(图9-4)。
细胞中微丝参与形成的结构除肌原纤维、微绒毛等属于稳定结构外,其他大都处于动态的组装和去组装过程中,并通过这种方式实现其功能。细胞松弛素(cytochalasin)可切断微丝纤维,并结合在微丝末端抑制肌动蛋白加合到微丝纤维上,特异性的抑制微丝功能。鬼笔环肽(phalloidin)与微丝能够特异性的结合,使微丝纤维稳定而抑制其功能。荧光标记的鬼笔环肽可特异性的显示微 丝。
二、微丝结合蛋白
已经分离出来的微丝结合蛋白有100多种,可分为以下不同类型(图9-5):
1.核化蛋白(nucleating protein)
核化(nucleation)是纤维组装的第一步,即几个蛋白单体先组装成多聚体,然后其它单体继续添加形成长纤维分子。Arp(actin-related protein)复合体在体内和体外都可以促进肌动蛋白的核化,其作用就像一个模板,类似于微管组织中心的γ球蛋白复合体,Arp复合体由Arp2、Arp3和5种其它蛋白构成。Arp与actin在结构上具有同源性。
2.单体隐蔽蛋白(monomer sequestering protein)
细胞中约有50%的肌动蛋白为可溶性肌动蛋白,大大高于肌动蛋白组装所需的临界浓度。但是这些蛋白与其它蛋白结合,构成一个隐蔽的蛋白库。只有当细胞需要组装纤维的时候这些可溶性肌动蛋白才被释放出来。如:thymosin与actin结合可阻止其向纤维添加,抑制其水解或交换结合的核苷酸。
3.封端蛋白(end-blocking protein)
作用是调节肌动蛋白纤维的长度,结合在(+)或(-)极形成“帽子”,阻止其它单体添加。如骨骼肌细肌丝的(-)端被tropomodulin封闭,(+)端被CapZ封闭。
4.单体聚合蛋白(monomer polymerizing protein)
如profilin结合在actin的ATP结合位点相对的一侧,能与thymosin竞争结合actin,profilin可将结合的单体安装到纤维的(+)极。
5.微丝解聚蛋白(actin-filament depolymerizing protein)
如cofilin可结合在纤维的(-)极,使微丝去组装。这种蛋白在微管快速组装和去组装的结构中具有重要的作用,涉及细胞的移动、内吞和胞质分裂。
6.交联蛋白(cross-linking protein)
每一种蛋白含有2至多个微丝结合部位,因此可以将2至多条纤维联系在一起形成纤维束或网络。分为成束蛋白和成胶蛋白两类,成束蛋白如:丝束蛋白(fimbrin)、绒毛蛋白(villin)和α-辅肌动蛋白(α-actinin),可以将肌动蛋白纤丝交联成平行排列成束的结构。成胶蛋白,如细丝蛋白(filamin)促使形成肌动蛋白微丝网。
7.纤维切断蛋白(filament severing protein)
此类蛋白能结合在微丝中部,将微丝切断。如溶胶蛋白(gelsolin)。
8.膜结合蛋白(membrane-binding protein)
如粘着斑蛋白(vinculin)可将肌动蛋白纤维量接在膜上,参与构成粘合带。
?
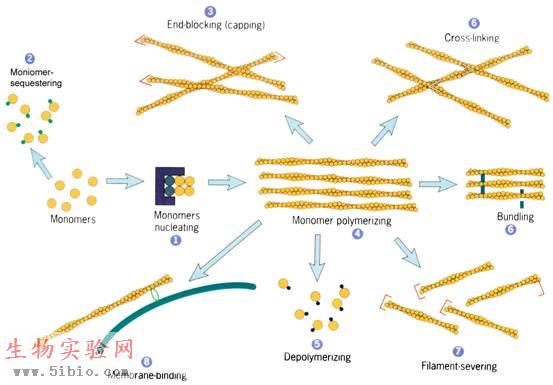
图9-5 各类微管结合蛋白(图片来自 G. Karp 2002)
三、肌肉的组成
肌肉由肌原纤维组成,肌原纤维由粗肌丝和细肌丝组成,粗肌丝的主要成分是肌球蛋白,而细肌丝的主要成分是肌动蛋白、原肌球蛋白和肌钙蛋白。关于肌小节的构造(图9-6、7)请参阅生理学或组织学书籍。
?

图9-6 肌纤维TEM照片
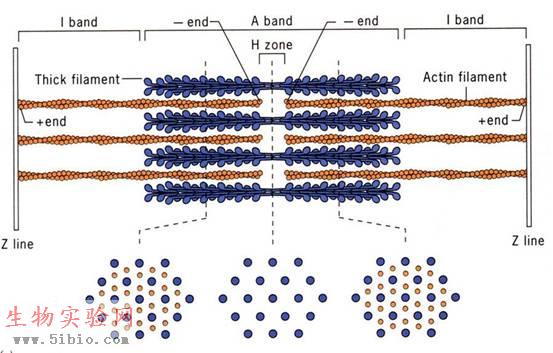
图9-7 肌小节模式图
(一)肌球蛋白(myosin)
属于马达蛋白,可利用ATP产生机械能,趋向微丝的(+)极运动(图9-8),最早发现于肌肉组织(myosin II),1970s后逐渐发现许多非肌细胞的myosin,目前已知的有15种类型(myosin I-XV)。
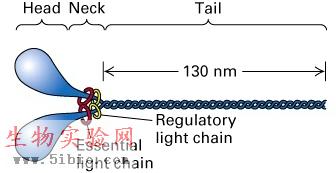
Myosin II是构成肌纤维的主要成分之一。由两个重链和4个轻链组成,重链形成一个双股α螺旋,一半呈杆状,另一半与轻链一起折叠成两个球形区域,位于分子一端,球形的头部具有ATP酶活性(图9-9)。
Myosin V结构类是于myosin II,但重链有球形尾部。
Myosin I 由一个重链和两个轻链组成。
Myosin I、II、V都存在于非肌细胞中,II型参与形成应力纤维和胞质收缩环,I、V型结合在膜上与膜泡运输有关,神经细胞富含myosin V 。

图9-8 myosin II 的功能
?
图9-9 myosin II结构模型
(二)原肌球蛋白
原肌球蛋白(tropomyosin.Tm)分子量64KD,是由两条平行的多肽链扭成螺旋,每个Tm的长度相当于7个肌动蛋白,呈长杆状。原肌球蛋白与肌动蛋白结合,位于肌动蛋白双螺旋的沟中,主要作用是加强和稳定肌动蛋白丝,抑制肌动蛋白与肌球蛋白结合(图9-10)。
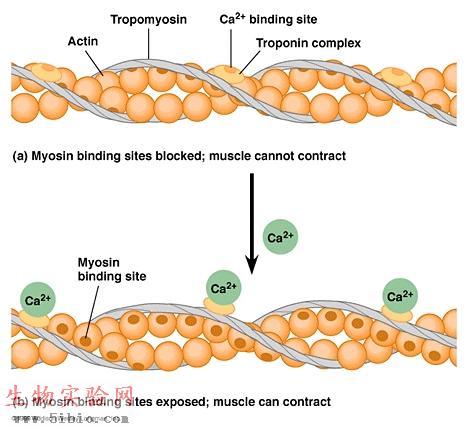
图9-10细肌丝的组成
(三)肌钙蛋白
肌钙蛋白(troponin,Tn),分子量80KD,含三个亚基,肌钙蛋白C特异地与钙结合,肌钙蛋白T与原肌球蛋白有高度亲和力,肌钙蛋白I抑制肌球蛋白的ATP酶活性,细肌丝中每隔40nm就有一个肌钙蛋白复合体(图9-8)。
(四)肌肉的收缩
肌细胞上的动作电位引起肌质网Ca2+电位门通道开启,肌浆中Ca2+浓度升高,肌钙蛋白与Ca2+结合,引发原肌球蛋白构象改变,暴露出肌动蛋白与肌球蛋白的结合位点(图9-8)。肌动蛋白通过结合与水解ATP、不断发生周期性的构象改变、引起粗肌丝和细肌丝的相对滑动。肌动蛋白的工作原理可概括如下:
①肌球蛋白结合ATP,引起头部与肌动蛋白纤维分离;②ATP水解,引起头部与肌动蛋白弱结合;③Pi释放,头部与肌动蛋白强结合,头部向M线方向弯曲(微丝的负极),引起细肌丝向M线移动;④ADP释放ATP结合上去,头部与肌动蛋白纤维分离。如此循环(图9-11)。
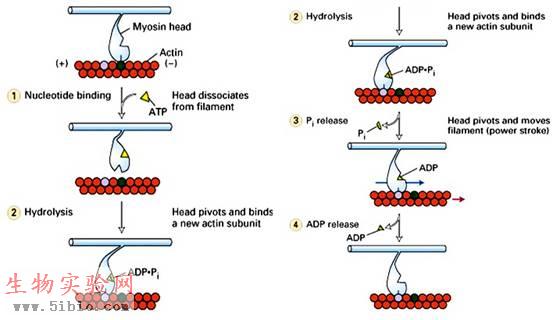
图9-11 肌肉收缩图解
四、微丝的功能
微丝除参与形成肌原纤维外还具有以下功能:
1.形成应力纤维(stress fiber):非肌细胞中的应力纤维与肌原纤维有很多类似之处:都包含myosin II、原肌球蛋白、filamin和α-actinin。培养的成纤维细胞中具有丰富的应力纤维,并通过粘着斑固定在基质上。在体内应力纤维使细胞具有抗剪切力(图9-12、13)。
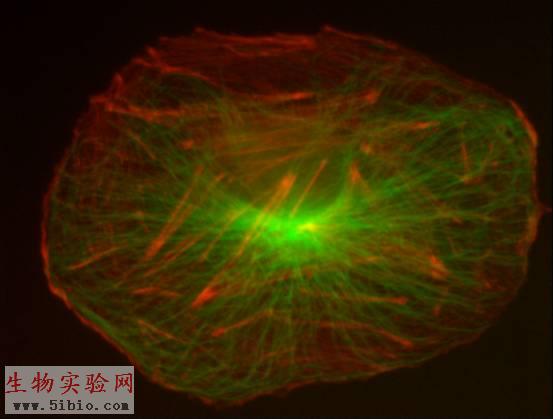
图9-12培养的上皮细胞中的应力纤维(微丝红色、微管绿色)(图片来自http://www.itg.uiuc.edu/)
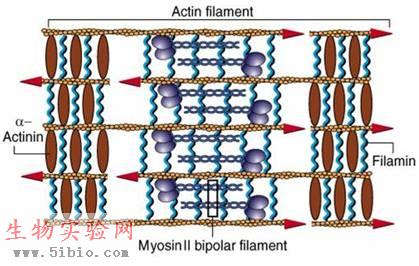
图9-13 应力纤维结构模型(图片来自 G. Karp 2002)
2.形成微绒毛:参见第四章。
3.细胞的变形运动:分为四步:①:微丝纤维生长,使细胞表面突出,形成片足(lamellipodium);②在片足与基质接触的位置形成粘着斑;③在myosin的作用下微丝纤维滑动,使细胞主体前移;④解除细胞后方的粘和点。如此不断循环,细胞向前移动(图9-14)。阿米巴原虫、白细胞、成纤维细胞都能以这种方式运动。

图9-14细胞的变形运动(根据Molecular Biology of the Cell 4th 书末动画改编)
4.胞质分裂:有丝分裂末期,两个即将分离的子细胞内产生收缩环,收缩环由平行排列的微丝和myosin II组成。随着收缩环的收缩,两个子细胞的胞质分离,在细胞松驰素存在的情况下,不能形成胞质分裂环,因此形成双核细胞。
5.顶体反应:在精卵结合时,微丝使顶体突出穿入卵子的胶质里,融合后受精卵细胞表面积增大,形成微绒毛,微丝参与形成微绒毛,有利于吸收营养。
6.其他功能:如细胞器运动、质膜的流动性、胞质环流均与微丝的活动有关,抑制微丝的药物(细胞松弛素)可增强膜的流动、破坏胞质环流。
共3页: 上一页 1 [2] [3] 下一页
|