1、溶质质量分数的概念:溶液中溶质的质量分数是溶质质量与溶液质量之比。
2、溶质的质量分数计算:溶液中溶质的质量分数可以用数学式表示如下:

3、溶液的稀释问题和浓缩问题:
①关于溶液稀释的计算:溶液稀释前后,溶质的质量不变,若设浓溶液质量为Ag,溶质的质量分数为a%,加水稀释成溶质的质量分数为b%的稀溶液Bg,则Ag×a%=Bg×b%(其中B=A+m水)
②关于溶液浓缩(无溶质析出)的计算――溶液浓缩通常有几种情况:
a、向原溶液中添加溶质:溶液增加溶质前后,溶剂的质量不变。增加溶质后,溶液中溶质的质量=原溶液中溶质的质量+增加的溶质的质量,而溶液的质量=原溶液的质量+增加的溶质的质量。若设原溶液质量为Ag,溶质的质量分数为a%,加溶质Bg后变成溶质的质量分数为b%的溶液,则Ag×a%+Bg=(Ag+Bg)×b%。
b、将原溶液蒸发去部分溶剂:溶液蒸发溶剂前后,溶质的质量不变。若设原溶液质量为Ag,溶质的质量分数为a%,蒸发Bg水后变成溶质的质量分数为b%的溶液,则:Ag×a%=(Ag一Bg)×b%。
c、与浓溶液混合:混合后的溶液的总质量等于两混合组分溶液的质量之和,混合后的溶液中溶质质量等于两混合组分的溶质质量之和。所以,设原溶液质量为Ag,溶质的质量分数为a%,浓溶液质量为Bg,溶质的质量分数为b%,两溶液混合后得到溶质的质量分数为c%的溶液,则:Ag×a%+Bg×b%=(Ag+Bg)×c%
常见考法
溶质质量分数的计算作为初中化学计算的重点和难点,是中考重点考查的内容。考查形式多样,选择、填空、实验、探究、推理、计算都曾有。解题关键是,找准所给溶液中溶质、溶剂或溶液的质量,没有溶解的不能计算在内。因此对溶质质量分数计算的正确理解和灵活运用十分重要。
主要题型有:计算溶液的溶质质量分数、计算配制溶液所需溶质和溶剂的质量、一定质量分数的溶液的配制、饱和溶液中溶质的质量分数的计算、溶液的稀释和浓缩、化学反应中有关溶质质量分数的计算。
误区提醒
1、关于溶液稀释一定要抓住:溶液稀释前后,溶质的质量不变。
2、关于溶液浓缩,要根据浓缩的具体类型来具体分析找出等量关系来解决。
3、溶质的质量分数只表示溶质质量与溶液质量之比,并不代表具体的溶液质量和溶质质量。
4、溶质的质量分数一般用百分数表示;是溶质质量占溶液质量的百分比,而不是体积关系。
5、溶质的质量分数数学表示式中溶质质量与溶液质量的单位必须统一。
【典型例题】
例析:
1、20℃时,KNO3的溶解度为31.6g,将20gKNO3投进50g水中,充分搅拌,制成20℃时的溶液,求该溶液中溶质的质量分数。
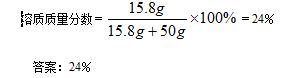
解析:
20℃时,100g水中最多能溶解KNO331.6g。则50g水中最多只能溶解15.8gKNO3,即20gKNO3中只有15.8gKNO3溶解,溶液就已饱和,还有4.2g不能溶解,不能看作溶液的组成部分。故:
2、向400g溶质的质量分数为4.9%的稀硫酸中加入足量的锌粒,充分反应后,求所得溶液中溶质的质量分数为多少?
解析:
[1] [2] 下一页
